Das gedruckte Heft ist ab Mitte April lieferbar. Vorbestellungen sind über den Warenkorb möglich.

© istockphoto / CocoSan
Ob Schokoriegel, Donuts oder andere süße Snacks – zucker- und fettreiche Lebensmittel sind aus unserem Alltag kaum wegzudenken. Sie sind lecker und praktisch, wir lieben sie als kleine Belohnung, schnellen Energiekick, Nervennahrung in stressigen Zeiten oder einfach als Genuss zwischendurch. Auch in vielen Fertigprodukten oder Fast Food stecken große Mengen an Zucker und Fett – ohne dass es uns bewusst ist. Warum aber können wir ausgerechnet solchen ungesunden Lebensmitteln kaum widerstehen?
Unser Körper verfügt über ausgeklügelte Mechanismen, um Energieverbrauch und -zufuhr auszutarieren. Die Schaltzentrale, die den Hunger kontrolliert, sitzt im Hypothalamus. Sie steht in engem Austausch mit dem Magen-Darm-Trakt, um von dort Informationen über den Energiegehalt und die Nährstoffzusammensetzung der Nahrung zu empfangen. Trotz dieses raffinierten Systems passiert es immer wieder, dass die Energiebilanz aus dem Gleichgewicht gerät: Wir essen, obwohl Energie im Überfluss vorhanden ist. Wie es dazu kommt, untersuchen der Neurowissenschaftler Marc Tittgemeyer und sein Team am Kölner Max-Planck-Institut für Stoffwechselforschung. Im Fokus der Forschenden steht die für uns unwiderstehliche Kombination „süß und fettig“. „Wir wollten herausfinden, warum wir ausgerechnet auf Fett und Zucker so stark reagieren“, sagt Tittgemeyer. Ist diese Vorliebe angeboren oder entsteht sie erst später im Leben, etwa infolge von bereits bestehendem Übergewicht? Oder ist unsere Lust auf Süßes und Fettiges womöglich erlernt? „Experimente lieferten Hinweise darauf, dass eine energiereiche Ernährung bei Mäusen zu einer Umprogrammierung bestimmter Schaltkreise im Gehirn führt und dadurch ein suchtartiges Verhalten hervorruft“, sagt der Wissenschaftler. Ob solche Effekte, die an Tieren beobachtet wurden, auch auf Menschen übertragbar sind, war jedoch unklar. Die Max-Planck-Forschenden entwarfen daher ein Experiment, um das zu überprüfen.
„Zucker und Fett sind typische Bestandteile von hochverarbeiteten Lebensmitteln“, sagt Marc Tittgemeyer. Die Wissenschaftlerinnen und Wissenschaftler untersuchten daher, wie sich der gewohnheitsmäßige Genuss solcher Nahrung auf unser Gehirn auswirkt. Dazu luden sie 49 normalgewichtige Personen zu einem achtwöchigen Experiment ein. Zu Beginn wurden die Teilnehmenden in zwei Gruppen eingeteilt: Eine Gruppe (A) aß zusätzlich zu ihrer normalen Ernährung jeden Tag zwei kleine, fett- und zuckerreiche Puddings. Die andere Gruppe (B) erhielt ebenfalls zwei Puddings, die weniger Fett und Zucker, dafür aber mehr Proteine enthielten (Abb. A). Der Kaloriengehalt der Puddings war in beiden Gruppen gleich. Zu Beginn und während der acht Wochen wurden regelmäßig Gewicht und Stoffwechselparameter wie Insulinresistenz und Blutfettwerte der Teilnehmenden kontrolliert. An bestimmten Testtagen bekamen beide Gruppen zusätzlich einen süßen, fettreichen Milchshake serviert. Mittels funktioneller Magnetresonanztomografie (fMRT, s. Kasten unten) maßen die Forschenden die Gehirnreaktionen ihrer Probandinnen und Probanden – einmal, während diese sich auf den Milchshake freuten und einmal, während sie ihn tranken. Dabei untersuchten sie verschiedene Hirnregionen, die mit dem dopaminergen System in Verbindung stehen, das für Antrieb und Motivation sorgt.
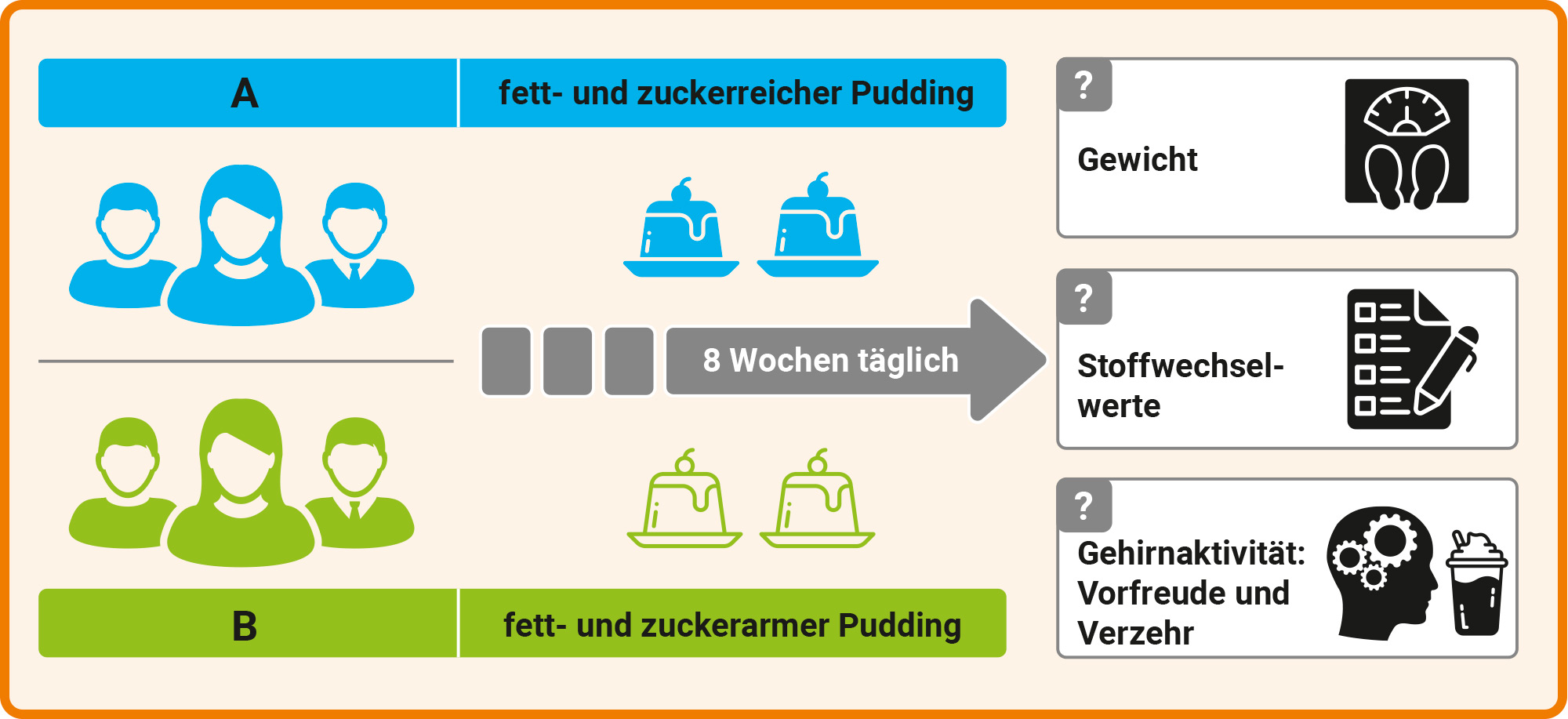
Abb. A: Die tägliche Dosis Fett und Zucker. Im Puddingexperiment untersuchten die Wissenschaftlerinnen und Wissenschaftler, wie sich der regelmäßige Konsum von fett- und zuckerreichen Lebensmitteln auswirkt.
© MPG
Nach Abschluss der Versuchsphase verglichen die Forschenden beide Gruppen: Bezüglich Gewicht und Stoffwechselparametern fanden sie keine auffälligen Veränderungen. Die Ergebnisse der fMRT-Untersuchungen fielen dagegen deutlich verschieden aus: Bei der Gruppe A, die den fett- und zuckerreichen Pudding bekommen hatte, waren beim Milchshake-Test die Gehirnreaktionen erhöht – und zwar sowohl während der Vorfreude als auch beim Verzehr des Milchshakes (Abb. B). Anhand eines Fragebogens stellten die Forschenden außerdem fest, dass in dieser Gruppe die Vorliebe für fettarme Lebensmittel deutlich abgenommen hatte.
„Unsere Messungen der Gehirnaktivität zeigen, dass sich durch den gewohnheitsmäßigen Konsum von fett- und zuckerreichen Lebensmitteln unser Gehirn tatsächlich neu verdrahtet“, erklärt Marc Tittgemeyer (s. BIOMAX 22). Durch diese antrainierten Veränderungen im Gehirn bevorzugen wir unbewusst weiterhin solche Lebensmittel, die viel Fett und Zucker enthalten. Eine wichtige Rolle spielt dabei das assoziative Lernen, das dopaminabhängig ist: Es bewirkt beispielsweise, dass wir das an sich neutrale Logo unserer Lieblingskonditorei damit assoziieren, dort einmal einen leckeren Donut gegessen zu haben. Allein der Anblick des Logos bewirkt dann, dass wir erneut einen Donut kaufen, obwohl wir eigentlich satt sind. All das passiert unbewusst.
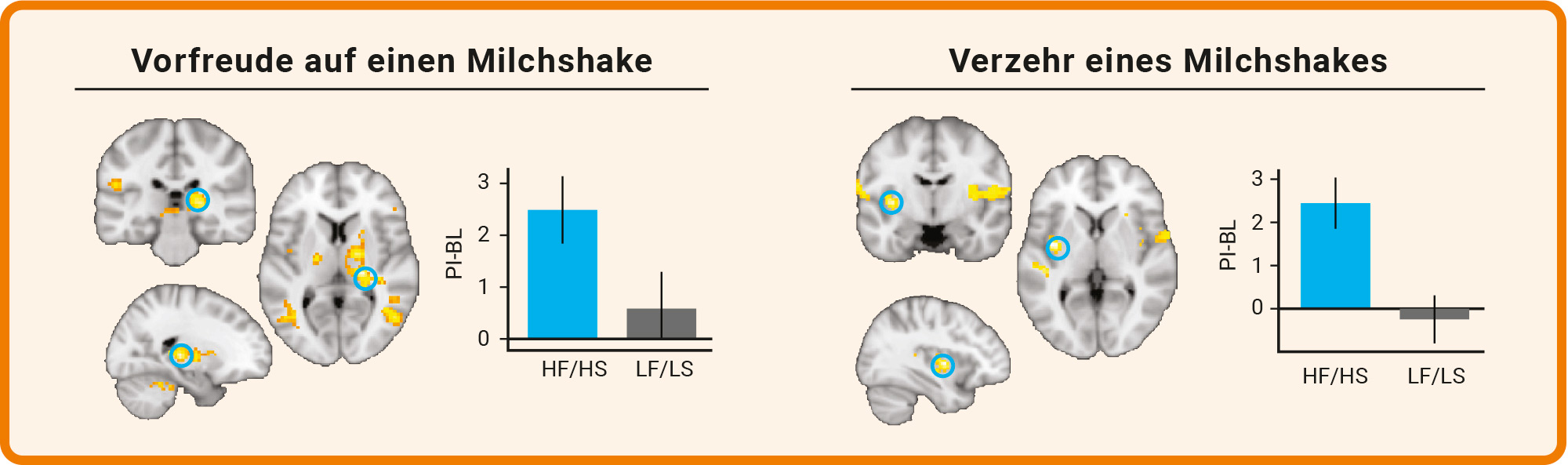
Abb. B: Veränderte Gehirnaktivität im fMRT. Links ist beispielhaft eine Region im Thalamus gezeigt, rechts im Kortex. Eine fett- und zuckerreiche Ernährung (high fat/high sugar; HF/HS) verstärkt die neuronalen Reaktionen (gelb mit blauem Kreis) in verschiedenen Teilen des Gehirns. Der PI-BL-Wert (Post-In-tervention-Baseline) ist ein Maß für die Veränderung der Gehirnaktivität. Die unterschiedliche Höhe der blauen und grauen Balken zeigt, dass das Gehirn nach einer HF/HS-Diät auf den Milchshake stärker anspricht als nach einer LF/LS-Diät (low fat/low sugar).
© MPI für Stoffwechselforschung
Warum aber reagiert unser Gehirn ausgerechnet auf die Kombination „süß und fettig“ so stark? „Im Fall von Zucker und Fett sind zwei unterschiedliche Signalwege beteiligt, die dem Gehirn die Verfügbarkeit dieser Nährstoffe melden. Diese beiden Signalwege kommen im dopaminergen Mittelhirn zusammen und verstärken sich dort auf fatale Weise gegenseitig. Lebensmittel, die eine solch starke Reaktion hervorrufen, essen wir besonders gerne“, sagt Marc Tittgemeyer. „Ich bin süchtig nach dieser Schokolade!“ ist daher mehr als nur ein Spruch, denn die Kombination „süß und fettig“ kann regelrecht rauschhafte Wirkung erzeugen und suchtartiges Verhalten auslösen: Wir wollen immer mehr davon. Im Laufe der Zeit kommt es dadurch zu einer Toleranzverschiebung – ein Prozess, bei dem der Körper nach wiederholter Zufuhr bestimmter Substanzen seine Stoffwechselvorgänge anpasst. Die Folge ist, dass wir die Dosis steigern müssen, um denselben Genuss zu empfinden wie am Anfang.
Was das Puddingexperiment anbelangt, nehmen die Forschenden an, dass die Vorliebe für Süßes und Fettiges auch über das Ende der Studie hinaus anhält: „Im Gehirn werden neue Verbindungen geknüpft, die sich auch nicht so schnell wieder auflösen. So wird die Vorliebe für , süß und fettig‘ gewissermaßen auf der Festplatte des Gehirns eingebrannt“, erklärt Marc Tittgemeyer. „Es ist daher auch unheimlich schwierig, sich dagegen zu wehren.“ Der Forscher geht jedoch davon aus, dass sich die Präferenz auch wieder in die andere Richtung verschieben lässt, wenn man über einen längeren Zeitraum hinweg seine Ernährungsgewohnheiten konsequent verändert.
Unser Antrieb, Zucker und Fett zu konsumieren, ist also bereits in den Signalwegen unseres Körpers angelegt. Wenn wir diese Kombination immer wieder zu uns nehmen, verstärken wir das Verlangen danach. Die Lebensmittelindustrie macht sich diesen Gewöhnungseffekt gezielt zunutze: Durch die optimale Mischung von Zucker mit Fett, Salz und Geschmacksverstärkern werden Produkte so entwickelt, dass sie das dopaminerge System besonders stark aktivieren. Welchen Effekt das hat, zeigt die Studie eines US-Forscherteams: Zwanzig normalgewichtige Personen hatten zwei Wochen lang hochverarbeitete Nahrung und weitere zwei Wochen selbst gekochtes Essen mit demselben Kaloriengehalt bekommen. Sie durften essen, soviel sie wollten. Nach Ende der Studie zeigte sich, dass die Probandinnen und Probanden mehr von der hochverarbeiteten Nahrung gegessen und dadurch zugenommen hatten.
Aus evolutionärer Sicht ist es sinnvoll und sogar überlebenswichtig, dass wir auf Zucker und Fett so stark reagieren. Die Anziehungskraft von Zucker hat ihren Ursprung möglicherweise in der fruchtbasierten Ernährung von Menschenaffen: Je süßer die Frucht, desto mehr Kalorien und damit Energie liefert sie. Die Vorliebe für „süß und fettig“ wird womöglich sogar schon im Säuglingsalter geprägt und buchstäblich mit der Muttermilch aufgesogen. „In der Steinzeit waren Lebensmittel mit hohem Kaloriengehalt selten zu finden. Es war daher vernünftig, jede Gelegenheit zu nutzen, um sich für schlechte Zeiten zu wappnen. Unser Gehirn verfügt deshalb auch über verschiedene Mechanismen, die dafür sorgen, dass wir über die Sättigungsgrenze hinaus essen können“, erklärt Marc Tittgemeyer.
Die meiste Zeit der Menschheitsgeschichte ging das gut: Hochverarbeitete Lebensmittel mit einer sehr hohen Kaloriendichte kamen erst mit dem wirtschaftlichen Aufschwung der 1960er- und 1970er-Jahre auf den Markt. Noch vor 200 Jahren war Zucker ein Luxusgut, das sich nur wohlhabende Menschen leisten konnten – ein seltener Genuss zu besonderen Gelegenheiten. Heute leben wir in einer Welt, in der Zucker allgegenwärtig ist: Unter etlichen unterschiedlichen Namen steckt er etwa als Saccharose, Fruktose oder Glukose nicht nur in Süßigkeiten und Getränken, sondern in auch in Fast Food und Produkten wie Salatdressing, Ketchup, Gewürzgurken, Fruchtjoghurt oder Müsli. Solche verarbeiteten Lebensmittel können zum Problem werden: „Die Evolution hat Chips und Donuts nicht vorgesehen“, resümiert Marc Tittgemeyer. „Große Zuckermengen können nach längerer Exposition die neuronalen Schaltkreise dauerhaft verändern und dysfunktionales Verhalten fördern, das zu Stoffwechselstörungen und Übergewicht führt.“ Auch Normalgewichtige sind davon betroffen, denn das Adipositas-Risiko kann bereits erhöht sein, wenn sich noch keine Veränderung im Körpergewicht zeigt. Ist erst einmal Übergewicht da, gerät man leicht in einen Teufelskreis: Je höher das Gewicht, desto resistenter wird der Stoffwechsel – mit der Folge, dass wir immer mehr essen. „Irgendwann deregulieren die Schaltkreise im Gehirn, und wir kommen nicht mehr dagegen an. Adipositas hat deshalb auch nichts mit Willensschwäche und Disziplinlosigkeit zu tun“, betont Tittgemeyer.
Weltweit nehmen Übergewicht und Adipositas rasant zu. In Deutschland ist bereits jeder sechste junge Mensch im Alter von drei bis 17 Jahren übergewichtig. Bei den Erwachsenen sind es zwei Drittel der Männer und die Hälfte der Frauen. Ein Viertel aller Erwachsenen gilt als adipös (BMI ≥ 30 kg/m2). Mögliche Folgen sind Typ-2-Diabetes, Herz-Kreislauf-Erkrankungen, Fettleber, Arthrose und verschiedene Krebsarten. Schätzungsweise geht jeder achte Todesfall in Europa auf Übergewicht und Adipositas zurück.
Ein Grund für die steigenden Zahlen ist der chronisch hohe Zuckerkonsum: Die Weltgesundheitsorganisation WHO empfiehlt, dass freie Zucker maximal 10 Prozent (besser 5 Prozent) der Gesamtenergiezufuhr ausmachen sollten. Unter freien Zuckern versteht man Mono- und Disaccharide, die Lebensmitteln zugesetzt werden, plus natürlich vorkommende Zucker in Honig, Sirupen, Fruchtsäften und -konzentraten. Der natürliche, in frischem Obst und Gemüse enthaltene Zucker zählt nicht dazu, weil dieser in eine Matrix aus Ballaststoffen „verpackt“ ist und daher langsamer aufgenommen wird. Bei einer Gesamtenergiezufuhr von 2000 kcal pro Tag für einen durchschnittlichen Erwachsenen entsprechen 10 Prozent einer Menge von 50 Gramm. Tatsächlich wird in Deutschland aber weit mehr Zucker konsumiert – am meisten von den 15- bis 24-Jährigen. Ein großer Anteil davon entfällt auf Fruchtsäfte, Nektare und Limonaden: 200 Milliliter eines solchen Getränks enthalten zwischen 20 und 34 Gramm Zucker.
Was lässt sich dagegen tun? Sind Süßstoffe wie Aspartam, Stevia oder Sucralose eine Lösung? Schließlich enthalten sie kaum oder keine Kalorien. Marc Tittgemeyer rät, auch solche Süßungsmittel sparsam zu verwenden. Ein Grund ist die sogenannte Antizipation – ein Signalweg, der den Nasen-Rachenraum mit dem Verdauungstrakt verbindet: „In Erwartung von Süßem schüttet die Bauspeicheldrüse Insulin aus, und die Leber beginnt mit der Lipolyse, sobald ich den ersten Bissen im Mund habe“, erklärt er. „Im Magen ist da noch gar nichts angekommen. Erwartet das Gehirn Zucker und der kommt nicht, sucht es nach Ausgleich und verlangt nach mehr.“ Süßstoffe helfen daher nicht, die Lust auf Süßes einzudämmen – im Gegenteil: Sie wirken sogar appetitanregend. Auch die Langzeitwirkung von Süßstoffen ist noch wenig erforscht. Süßungsmittel wie Agavendicksaft oder Dattelpulver enthalten viel Fruktose und sind daher ebenfalls problematisch: „Fruktose wird in der Leber direkt in Fett umgewandelt und führt auch schnell zur Entwicklung von Diabetes“, erklärt der Forscher.
Wie aber lässt sich der hohe Zuckerkonsum dann eindämmen? Wichtig sei eine umfassende Prävention von Anfang an: „Eltern sollten ihre Kinder und sich selbst gesund ernähren“, sagt Tittgemeyer. Eine aktuelle Studie deutet darauf hin, dass eine Zuckerreduktion in der Schwangerschaft und in den ersten beiden Lebensjahren hilft, bei Kindern das spätere Risiko für Typ-2-Diabetes und Bluthochdruck zu senken. Doch auch die Politik sei gefragt: Werbeverbote, ein Symbolsystem, um den Zuckergehalt von Lebensmitteln transparent zu machen oder die Einführung einer Zuckersteuer könnten helfen. Eine solche Steuer ist so angelegt, dass sie mit zunehmendem Zuckergehalt eines Produkts ansteigt. Das soll die Industrie dazu bewegen, ihre Rezepturen zu verändern. In vielen Ländern der Welt gibt es eine Zuckersteuer bereits, vor allem auf Softdrinks.
Unabhängig von politischen Entscheidungen haben wir es auch selbst in der Hand, wie wir mit Zucker umgehen. Da sich unser Stoffwechsel durch dauerhaft hohen Zuckerkonsum unbemerkt verändert und schleichend aus dem Lot geraten kann, ist Vorbeugung so wichtig: „Das heißt nicht, dass wir uns ständig in Verzicht üben müssen. Die Dosis macht das Gift“, sagt der Forscher, der selbst gerne ab und zu Süßes isst. „Süßigkeiten sollten daher etwas Besonderes bleiben.“ Er rät, sparsam mit Softdrinks, hochverarbeiteten Lebensmitteln und Fast Food umzugehen und stattdessen mehr selbst zu kochen und bewusst zu genießen.
Um die Gehirnaktivität der Personen während des Milkshake-Tests zu messen, verwendeten die Forschenden die funktionelle Magnetresonanztomografie (fMRT). Mithilfe dieses Untersuchungsverfahrens lässt sich feststellen, welche Bereiche im Gehirn gerade besonders aktiv sind. Es beruht auf dem sogenannten BOLD-Kontrast (Blood Oxygen Level Dependent): Aktive Nervenzellen verbrauchen Energie und benötigen Sauerstoff. Wenn ein bestimmter Hirnbereich aktiv ist, fließt daher mehr sauerstoffreiches Blut dorthin. Da sauerstoffbeladenes Hämoglobin andere magnetische Eigenschaften hat als sauerstofffreies Hämoglobin, lässt sich dieser Blutfluss in einem starken Magnetfeld sichtbar machen. Der Computer verrechnet die verschiedenen Signale zu einem farbigen Bild (Grundlagen zur MRT s. TECHMAX 33) . Das Foto zeigt eine Kopfspule, die Aufnahmen mit hoher Präzision ermöglicht.
Foto © Arne Sattler, MPIB
Abbildungshinweise:
Titelbild: © istockphoto / CocoSan
Abb. A: © MPG
Abb. B: © MPI für Stoffwechselforschung
Kasten: © Arne Sattler, MPIB
Der Text wird unter CC BY-NC-SA 4.0 veröffentlicht.
BIOMAX Ausgabe 41, März 2026; Text: Dr. C. Pietschmann, Dr. E. Maier; Redaktion: max-wissen-Team
Jedes wild lebende Tier steht Tag für Tag vor der Herausforderung, genügend Futter zu finden. Dabei schwanken die zur Verfügung stehenden Futter-Ressourcen im Lauf des Jahres sehr stark: Die Waldspitzmaus hat eine einzigartige Strategie, um mit diesen Veränderungen umzugehen: Im Winter, wenn das Nahrungsangebot knapp ist, schrumpfen ihr Schädel und mit ihm ihr Gehirn sowie einige andere Organe deutlich. Das hilft ihr, Energie zu sparen. Wird es wärmer, wachsen Schädel, Gehirn und Organe wieder. Und das ist längst nicht alles, was die Spitzmaus so besonders macht! Dina Dechmann vom Max-Planck-Institut für Verhaltensbiologie gibt einen Einblick in das einzigartige Leben der kleinen Raubtiere.
Audiodatei | 20 min, Mai 2024
© MPG / CC BY-NC-ND 4.0
Aus Wind und Sonne erzeugte Elektrizität ist die Hauptalternative zu fossilen Energieträgern. Bislang gab es jedoch keine Möglichkeit, elektrischen Strom direkt in biochemische Reaktionen einzuspeisen. Tobias Erb und seinem Team ist nun ein Durchbruch gelungen: Sie haben eine Enzymkaskade entwickelt, die mithilfe elektrischen Stroms ATP herstellen kann. Dieses lässt sich zur Bildung energiereicher chemischer Verbindungen nutzen, wie zum Beispiel zur Produktion von Stärke und Proteinen. Wie dies funktioniert, erklärt der Kurzfilm.
[Dauer des Videos: 3 min]

© wachiwit/Adobe Stock
Unser gesamtes Leben baut auf Fotosynthese auf. Die musste sich im Laufe der Zeit an große Veränderungen in der Umwelt anpassen. Eine neue Studie zeigt, wie dies das Enzym Rubisco geschafft hat und was die Erkenntnis darüber für die zukünftige Fotosynthese und auch unser Klima bedeuten kann.
Themen im Podcast: Enzym Rubisco / Fotosynthese / Anpassungen der frühen Fotosynthese / Rubisco-Varianten / Proteinstammbaum / Opitimierung Rubisco
Zum Podcast vom 24. Oktober 2022 (13 min) © detektor.fm/Max-Planck-Gesellschaft
Eine Herausforderung des 21. Jahrhunderts ist die Eindämmung des Klimawandels. Und das heißt, dass es uns gelingen muss, den Anteil von Treibhausgasen in der Atmosphäre zu reduzieren. Kohlenstoffdioxid aus der Luft mithilfe von Sonnenenergie nutzbar machen – diesen Prozess beherrschen Pflanzen bereits seit Jahrmillionen. Eröffnet die künstliche Fotosynthese einen Weg, um aus Kohlenstoffdioxid mithilfe von Licht nachhaltig Rohstoffe zu produzieren? Ein Team um Tobias Erb, Direktor am Max-Planck-Institut für terrestrische Mikrobiologie in Marburg, arbeitet daran, diesen Prozess so zu „tunen“, dass er mehr Kohlenstoff binden kann. Mit ihrem synthetisch-biologischen Ansatz wollen die Max-Planck-Forschenden biologische Prozesse jedoch nicht nur schrittweise verbessern, sondern auch ganz neue Lösungen umsetzen, die in dieser Form in der Natur nicht zu finden sind – eine Idee mit vielversprechendem Potenzial.
Jedes Jahr holen Fotosynthese treibende Organismen rund 400 Gigatonnen Kohlenstoffdioxid (CO2) aus der Luft. Im natürlichen Kohlenstoffkreislauf entsprach das genau der Menge an CO2, die durch geologische und biologische Prozesse wieder freigesetzt wurde – bis mit Beginn des Industriezeitalters (etwa um 1750) der Mensch anfing, zunehmend fossile Brennstoffe wie Kohle, Erdöl und Erdgas, in denen der Kohlenstoff aus Jahrtausenden bis Jahrmillionen unterirdisch gespeichert war, zu verbrennen. Dadurch bringen wir den Kohlenstoffkreislauf zunehmend aus dem Gleichgewicht: Aktuell emittieren wir jährlich 38 Gigatonnen CO2 zusätzlich, also knapp ein Zehntel des natürlichen Kreislaufs (siehe GEOMAX 22). Ein Verfahren, welches das überschüssige Kohlenstoffdioxid wieder aus der Atmosphäre entfernt und gleichzeitig noch sinnvoll nutzt, wäre also hochwillkommen. Tobias Erb, Direktor am Max-Planck-Institut für terrestrische Mikrobiologie treibt aber nicht primär der Kampf gegen den Klimawandel an. Zunächst einmal will er verstehen, wie sich Kohlenstoffdioxid in organische Moleküle umwandeln lässt. „Wenn wir das Treibhausgas mit biologischen Methoden als Kohlenstoffquelle erschließen und dabei aus der Atmosphäre entfernen könnten, wäre das natürlich ein toller Nebeneffekt“, sagt der Max-Planck-Forscher.
Evolutionär betrachtet ist die Fotosynthese ein ausgesprochen erfolgreicher biochemischer Prozess und sehr gut in der Lage, die Anforderungen der biologischen Funktionen zu erfüllen: Einfach zusammengefasst, wandelt sie das CO2 aus der Luft mithilfe von Sonnenenergie und Wasserstoff in Kohlenhydrate um. Um Wasserstoff zu gewinnen, müssen Pflanzen dabei Wassermoleküle spalten. Den überschüssigen Sauerstoff gibt die Pflanze an die Umwelt ab. Ein Teil der Kohlenhydrate liefert die nötige Energie zum Leben, der andere Teil wird zum Grundbaustein für die Produktion großer Biomoleküle. Mit diesen wächst die Biomasse an – die Pflanze speichert so den Kohlenstoff aus der Atmosphäre.
Der Prozess hat aber auch seine Grenzen. So beträgt die Effizienz der Umwandlung von eingestrahltem Sonnenlicht in Biomasse bei der biologischen Fotosynthese (ohne den Eigenverbrauch der Pflanze) gerade mal ein Prozent. Das ist nichts im Vergleich zu gängigen Fotovoltaikanlagen, die rund 20 Prozent der eingesammelten Sonnenenergie in elektrische Energie umwandeln. Ein Flaschenhals für die Effizienz ist die Transpiration der Pflanzen. Über die Spaltöffnungen der Blätter, die sogenannten Stomata, nehmen Pflanzen nicht nur das CO2 aus der Luft auf, sondern verdunsten dabei gleichzeitig auch Wasser. Die Verdunstung verbraucht jedoch wesentlich mehr Wasser als die Fotosynthese-Reaktion. Indem die Pflanze den Verlust an Wasser begrenzt, schränkt sie auch den Gasaustausch und die Fotosyntheseleistung ein.
Als einen weiteren limitierenden Faktor hat Axel Kleidon, Forschungsgruppenleiter am Max-Planck-Institut für Biogeochemie, die Thermodynamik ausgemacht. Als Erdsystemforscher untersucht er wichtige chemische, geologische und physikalische Prozesse und Stoffkreisläufe auf der Erde. Das erfordert einen Blick auf das Große und Ganze: „Der CO2-Transport an die Blätter erfolgt durch die große Umwälzanlage der Thermik, indem erwärmte, befeuchtete und CO2-ärmere Luft vom Boden aufsteigt und kühlere, trockenere und CO2-reichere Luft absinkt“, erklärt Kleidon. Der Motor dafür ist die Erwärmung der Erdoberfläche durch die Sonnenstrahlung. Dadurch entsteht ein Temperaturunterschied, der eine atmosphärische Wärmekraftmaschine antreibt. „Diese Maschine leistet so viel wie möglich, sie begrenzt aber auch die Verdunstung und damit den Nachschub an CO2 für die Fotosynthese“, so der Physiker. Denn der Wärmefluss, der die Maschine antreibt, baut auch den Temperaturunterschied wieder ab und reduziert so ihren Wirkungsgrad. Die biologische Fotosynthese ist also immer nur so effektiv, wie der thermodynamisch geleistete Nachschub. „Natürliche Ökosysteme und auch die Landwirtschaft operieren schon nah an ihrer Leistungsgrenze, substanzielle Steigerungen sind hier kaum zu erwarten“, betont Kleidon daher.

Abb. D: Der heutige Chloroplast hat sich in 3,5 Milliarden Jahren zu einer effizienten molekularen Maschine entwickelt.
© Science History Images / Alamy Stock

Abb. D: Der künstliche Chloroplast wurde in weniger als 7 Jahren entworfen und realisiert (grün: Thylakoidmembranen).
© T. Erb / MPI für terrestrische Mikrobiologie
Die Biologie lässt sich nicht weiter optimieren, wenn die Physik ihr Grenzen setzt. Aber die heute gut erforschten fotosynthetischen Prozesse in Pflanzen, Algen und Bakterien können als Vorbild dienen für die Entwicklung einer künstlichen Fotosynthese. Der künstliche Nachbau der Fotosynthese gilt dabei als eine Art „Apollo-Projekt“ unserer Zeit: Damit ließen sich Kohlenstoffverbindungen nachhaltig mithilfe von Licht aus Kohlenstoffdioxid herstellen. Sonnenlicht wäre dafür die ultimative Ressource, denn die Sonne sendet ungefähr 15.000-mal mehr Energie zur Erde als die Menschheit verbraucht. Die technische Umsetzung der beiden Teilprozesse der Fotosynthese, der Primär– und der Sekundärreaktion, befindet sich dabei in unterschiedlichen Entwicklungsstadien. Für die Primärreaktion wurden fotovoltaische Lösungen realisiert, die hinsichtlich der Photonenausbeute dem natürlichen Prozess entsprechen. Für die technische Umsetzung der Sekundärreaktion konnte bisher keine mit dem natürlichen System konkurrierende katalytische Lösung gefunden werden. Doch genau das ändert sich gerade – dank der Forschungsarbeiten von Tobias Erb.
Die Umwandlung von atmosphärischem CO2 in energetisch höherwertige Kohlenstoffverbindungen erfolgt in Pflanzen über den nach seinem Entdecker benannten Calvin-Zyklus. Der US-amerikanische Biochemiker Melvin Calvin verfolgte mit seiner Arbeitsgruppe an der University of California in Berkeley Ende der 1940er Jahre, wie aus radioaktiv markiertem Kohlenstoffdioxid in einem Kreisprozess Kohlenhydrate hergestellt wurden. 1961 erhielt er für diese Arbeiten den Nobelpreis für Chemie. Für den Ablauf der chemischen Reaktionen, die im Stroma der Chloroplasten stattfinden, werden als Voraussetzung lediglich ATP als Energiequelle und NADPH/H+ als Reduktionsmittel benötigt. Das zentrale Enzym, das die Bindung von CO2 katalysiert, heißt Ribulose-1,5-bisphosphatcarboxylase/-oxygenase, kurz Rubisco (Abb. A). Es ist eines der häufigsten Proteine der Natur. „Nimmt man das Proteom, also alle Proteine zusammengefasst in einem Blatt, so besteht das zu fünfzig Prozent aus Rubisco“, erklärt Tobias Erb.

Abb. A: Das CO2-bindende Enzym des Calvin-Zyklus heißt Rubisco. Es ist sehr komplex gebaut und besteht aus 16 Untereinheiten. Auf jeden Menschen kommen etwa fünf Kilogramm Rubisco. Aus dem Kohlenstoffdioxid, das im Volumen eines gewöhnlichen Wohnzimmers vorhanden ist, kann die Pflanze mithilfe des Enzyms eine Prise Zucker produzieren.
© Grafik: A. Bracher / MPI für Biochemie
Dabei ist Rubisco keine optimale Lösung, wenn es um die Effizienz der Kohlenstofffixierung geht. Denn trotz seiner wichtigen Rolle arbeitet Rubisco relativ langsam: Ein Molekül kann nur etwa fünf bis zehn CO2-Moleküle in der Sekunde umsetzen. Und es ist sehr ineffizient, da es nicht nur CO2 bindet, sondern auch Sauerstoff. Als Rubisco vor rund drei Milliarden Jahren entstand, war das noch kein Problem – da gab es nämlich noch keinen Sauerstoff in der Atmosphäre. Als sich dieser jedoch mehr und mehr anreicherte, konnte sich das Enzym dieser Veränderung nicht anpassen. Zwanzig Prozent der Reaktionen laufen unerwünscht mit dem Sauerstoff ab. Die Pflanzenzelle kann mit dem daraus entstehenden toxischen Produkt nichts anfangen. Sie muss es in einem aufwändigen Prozess, der sogenannten Photorespiration, umwandeln, wobei wiederum CO2 freigesetzt wird. Dieser Prozess verpulvert bis zu einem Drittel der durch die Fotosynthese eingefangenen Energie – was die Pflanzen sich aber angesichts der unbegrenzten Verfügbarkeit von Sonnenenergie leisten können.
Tobias Erb setzt derweil auf eine effizientere Alternative zu Rubisco, die er vor einigen Jahren mit seinem Team im Bodenbakterium Kitasatospora setae entdeckt hat. Das betreibt zwar keine Fotosynthese, musste aber lernen, seinen Bedarf an Kohlenstoff in einer kohlenstoffarmen Umwelt zu decken. Dazu entwickelte dieses Bakterium eine höchst wirksame Klasse von Enzymen mit dem Namen Enoyl-CoA Carboxylase/Reduktase, kurz ECR. Sie können das Kohlenstoffdioxid etwa zwanzigmal schneller verarbeiten als das pflanzliche Rubisco – nicht zuletzt deshalb, weil dabei auch kaum Fehler auftreten.
Dieser Fund brachte Erb auf die Idee, eine künstliche, hocheffiziente Alternative zum Calvin-Zyklus quasi neu zu erfinden und dabei Hochleistungsenzyme wie ECR zu nutzen. Die Herausforderung bestand darin, dass an dem Prozess noch ein gutes Dutzend anderer Enzyme beteiligt sind, die fein aufeinander abgestimmt sein müssen. Entfernt man auch nur eines davon, dann bricht der biochemische Prozess zusammen. „Das Enzym ist eigentlich nur so etwas wie ein neues Computerprogramm“, erklärt Erb. „Damit es aber funktioniert, mussten wir – um im Bild zu bleiben – ein komplettes neues Betriebssystem aufbauen.“ Dazu suchte das Team Enzyme zusammen, die jeweils ihre Aufgabe im „Betriebssystem“ möglichst optimal erledigen (Abb. B). Sie fanden sich in so unterschiedlichen Organismen wie Purpurbakterien, Gänserauke und sogar der menschlichen Leber. Einige Enzyme mussten auch chemisch umgebaut werden. Das Ergebnis nennt sich „CETCH-Zyklus“. Es ist der erste künstliche Stoffwechselweg zur biologischen CO2-Fixierung. Mit 15 bis 17 Einzelschritten ist er vergleichbar komplex wie sein natürliches Vorbild, arbeitet aber wesentlich effizienter und zudem fehlerfrei: Theoretische Berechnungen zeigen, dass der CETCH-Zyklus lediglich 24 bis 28 Lichtquanten pro fixiertem, also gebundenem CO2-Molekül benötigt. Verglichen mit der natürlichen Sekundärreaktion in Pflanzen (ca. 34 Lichtquanten pro CO2-Molekül) braucht der künstliche Stoffwechselweg damit bis zu 20 Prozent weniger Lichtenergie. Im Reagenzglas sei der Designer-Stoffwechselweg bereits funktionsfähig, so der Max-Planck-Forscher. Zu den aufgereinigten Proteinen, die beteiligt seien, müsse man noch ATP als Energielieferant hinzugeben, und der CETCH-Zyklus laufe los.
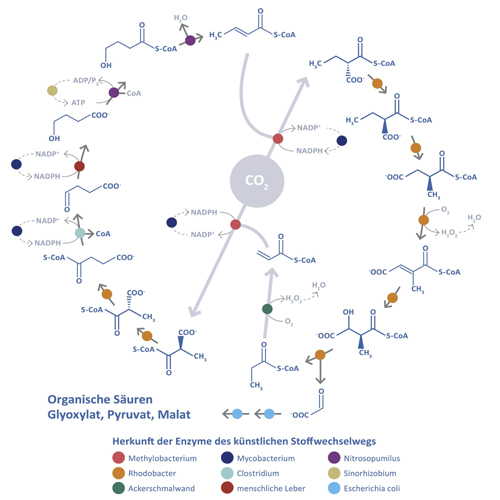
Abb. B: Entwurf und die Realisierung künstlicher Stoffwechselwege zur effizienteren CO2-Reduktion mithilfe der synthetischen Biologie: Der CETCH-Zyklus besteht aus 17 verschiedenen Enzymen, die aus insgesamt neun verschiedenen Organismen (farblich gekennzeichnet) stammen. Drei dieser Enzyme wurden mit Computerunterstützung maßgeschneidert, um eine entsprechende Reaktion zu katalysieren.
© acatech / Leopoldina / Akademienunion auf Grundlage von T. Erb
Praktisch musste das Marburger Team dies erst einmal in einem künstlichen Fotosynthesesystem beweisen. Doch wie konstruiert man eine künstliche fotosynthetisch aktive Zelle? „Als allererstes benötigten wir ein Energiemodul, das es uns erlaubt, chemische Reaktionen nachhaltig zu betreiben. Bei der Fotosynthese liefern Chloroplasten-Membranen die Energie für die Kohlenstoffdioxid-Fixierung. Ihre Fähigkeiten wollten wir nutzen“, erklärt Erb. Der aus der Spinatpflanze isolierte Fotosynthese-Apparat zeigte sich robust genug, um auch im Reagenzglas die Energie aus dem Licht, die Elektronen und den Wasserstoff bereitzustellen. Für die Sekundärreaktion setzten die Forschenden den von ihnen selbst entwickelten CETCH-Zyklus ein (Abb. D). Nach mehreren Optimierungsrunden gelang dem Team tatsächlich die lichtgesteuerte Fixierung des Treibhausgases Kohlenstoffdioxid in vitro. „Mit der Plattform können wir neuartige Lösungen umsetzen, die die Natur während der Evolution nicht beschritten hat“, sagt Erb. Nach seiner Einschätzung bergen die Ergebnisse großes Zukunftspotenzial. So konnten die Forschenden zeigen, dass der künstliche Chloroplast mithilfe der neuartigen Enzyme und Reaktionen Kohlenstoffdioxid 100-mal schneller bindet als bisherige synthetisch-biologische Ansätze. „Langfristig könnten lebensechte Systeme in praktisch allen technologischen Bereichen Anwendung finden, einschließlich Materialwissenschaften, Biotechnologie und Medizin“, hofft der Max-Planck-Forscher.
Noch sind die künstlichen Chloroplasten nur feine Wassertröpfchen von knapp 100 Mikrometern Durchmesser, die in einer Ölemulsion schwimmen (Abb. C). Sie sind nur zwei Stunden lang stabil. Trotzdem können sie erstaunlicherweise selbstständig aus dem gebundenen Kohlenstoff messbare Mengen der Verbindung Glykolat herstellen. Daraus lassen sich bereits eine Vorstufe des Antibiotikums Erythromycin oder ein Duftstoff auf Terpen-Basis herstellen, wie Erbs Team zeigen konnte.
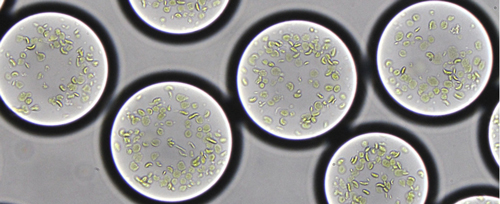
Abb. C: Diese Tröpfchen haben 90 Mikrometer Durchmesser und sind ein Beispiel für halb künstliche Chloroplasten aus Marburg. Sie enthalten bereits Thylakoidmembranen aus echten Chloroplasten, in denen die Primärreaktion der Fotosynthese abläuft. © T. Erb / MPI für terrestrische Mikrobiologie; CC BY-NC-SA 4.0
Alternativ zum rein künstlichen Fotosynthesesystem forscht das Team auch daran, die Enzyme für den CETCH-Zyklus gentechnisch in lebende Zellen einzubauen. „In E. coli-Bakterien ist uns das bereits zu neunzig Prozent gelungen“, berichtet Tobias Erb. Der nächste Schritt ist der gentechnische Einbau des CETCH-Zyklus in den Stoff-wechsel einzelliger Algen – eine viel größere Herausforderung, da sie weitaus weniger erforscht sind als E. coli und deutlich komplexere Zellstrukturen besitzen. Außerdem ist die Entwicklung synthetischer Algenstämme durch ihre niedrigere Wachstumsrate langwieriger. Gelingt der Einbau, so wären große „Algenfabriken“ denkbar, die CO2 besonders effektiv in Biomasse umwandeln können. Das wäre dann tatsächlich ein Schritt hin zur Bewältigung einer der größten Herausforderungen unserer Zeit: die Reduktion der ständig steigenden Konzentration von atmosphärischem Kohlenstoffdioxid.
Abbildungshinweise:
Titelbild: © S. Peterman / Adobe Stock; MPI für terrestrische Mikrobiologie
Abb. A: © Grafik: A. Bracher / © MPI für Biochemie
Abb. B: © Grafik auf Grundlage von T. Erb; acatech/Leopoldina/Akademienunion (Hrsg.): Künstliche Photosynthese. Forschungsstand, wissenschaftlich-technische Herausforderungen und Perspektiven, München 2018.
Abb. C: © T. Erb, MPI für terrestrische Mikrobiologie / CC-BY-NC-SA 4.0
Abb. D: links © Science History Images / Alamy Stock; rechts © T. Erb, MPI für terrestrische Mikrobiologie / CC-BY-NC-SA 4.0
Der Text wird unter CC BY-NC-SA 4.0 veröffentlicht.
BIOMAX 37, Frühjahr 2022; Text: Christina Beck, Roland Wengenmayr; Redaktion: Tanja Fendt
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
YouTube-Link: https://youtu.be/ynfIBOhJdUc
In „Stowaway“ bringt ein blinder Passagier die Crew eines zum Mars fliegenden Raumschiffs in Lebensgefahr. Durch einen technischen Defekt gibt es zu wenig Sauerstoff für die nun zu große Besatzung.
Algen-Experte Wojciech Wietrzynski vom Max-Planck-Institut für Biochemie war bei der Produktion des Kinofilms „Stowaway – Blinder Passagier“ unterstützend am Filmset dabei. Im Stowaway-Raumschiff schicken wir nun @Doktor Whatson auf den Mars :)! Als wissenschaftliche Begleitung sind Wojciech und Dominique Segura-Cox vom Max-Planck-Institut für extraterrestrische Physik mit an Bord.
**** Spoiler-Alarm ****
In dieser Filmbesprechung werden u. a. Szenen aus dem Kinofilm „Stowaway“ diskutiert.
**** Spoiler-Alarm ****
Englische Originalversion dieses Youtube-Videos:
https://youtu.be/Vjni0cTAZ9I
The original English version of this Youtube video may be found here:
https://youtu.be/Vjni0cTAZ9I
In Kooperation mit der Max-Planck-Gesellschaft ist auch das Video „Hollywood wissenschaftlich geprüft | Wissenschaftler Reagieren auf Stowaway Teil 1“ entstanden @Doktor Whatson: https://youtu.be/eCZqi2U-N9c
[Dauer des Videos: 24 min]
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.