„Ich bin total im Stress!“ – wer hat das nicht schon oft gehört. Lernstress vor Prüfungen, Termindruck im Job, Social Media – manchmal wird es einfach zu viel. Aber was passiert da eigentlich in unserem Körper? Warum fühlen sich manche Menschen gestresster als andere? Und: Wie bleibt man mental gesund? Mathias V. Schmidt vom Max-Planck-Institut für Psychiatrie spricht mit Wissenschaftsjournalistin Alice Lanzke über Erkenntnisse aus der Stressforschung.
Audiodatei | 20 min, August 2025
© MPG / CC BY-NC-ND 4.0
„Ich bin total im Stress!“ – wer hat das nicht schon oft gehört. Ob in Schule, Studium oder Beruf: Lernstress vor Prüfungen, Termindruck im Job und manchmal sogar Freizeitstress, wenn man sich unter der Woche zu viel vorgenommen hat. Stress hat in unserer Gesellschaft ein ausgesprochen schlechtes Image. Zu Recht? „Ohne Stress wäre unser Leben ziemlich langweilig“, sagt der Biologe Mathias V. Schmidt vom Max-Planck-Institut für Psychiatrie in München. „Wir könnten unseren Alltag gar nicht bewältigen, wenn es keinen Stress gäbe und wir kein funktionierendes Stresssystem hätten.“
Stress ist also per se nichts Negatives. Das Stresshormon Cortisol etwa hilft uns dabei, morgens überhaupt aufstehen zu können – zu diesem Zeitpunkt ist die Cortisol-Konzentration im Blut erhöht. Sie sorgt dafür, dass wir mit Energie in den Tag starten. Abends sinkt sie wieder, damit wir zur Ruhe kommen. „Im Grunde helfen uns Stressreaktionen dabei, die ganz normalen Herausforderungen des Alltags zu bewältigen. Stress gehört zum Leben dazu“, sagt Mathias V. Schmidt. Problematisch wird es, wenn wir zu viel Stress haben – und zwar in Bezug auf Intensität und Dauer (Abb. A). Hält Stress zu lange an, kann unser Stoffwechsel nicht mehr in den Normalzustand zurückkehren. Ein solcher Dauerstress kann krank machen und psychische Erkrankungen wie zum Beispiel Depressionen auslösen. Auch besonders intensiver Stress, etwa durch traumatische Erlebnisse, kann zu solchen Erkrankungen führen. Mathias V. Schmidt untersucht unter anderem an Mäusen, wie verschiedene Arten von Stress auf Säugetiere wirken. Mäuse sind dafür gut geeignet, weil ihr Stresshormon-System und die Rezeptoren – die Andockstellen für Stresshormone in ihrem Gehirn – denen des Menschen sehr ähnlich sind. In seiner Forschung hat der Biologe unter anderem herausgefunden, dass sozialer Stress bei Mäusen einer der stärksten Stressoren überhaupt ist.

Abb. A: Ursachen von Stress. Auszug einer Befragung von volljährigen Personen in Deutschland im Frühjahr 2021: Große Stressfaktoren sind – wie schon vor der Corona-Pandemie – das Pensum an Anforderungen von Schule, Studium und Beruf sowie hohe Ansprüche an sich selbst. Stark an Bedeutung gewonnen hat durch die Pandemie die Sorge um erkrankte Nahestehende. Weitere Ursachen siehe Quelle.
© Quelle Zahlen: Techniker Krankenkasse (TK-Stressstudie, 2021); Grafik: HNBM
Sozialer Stress macht Mäuse vor allem dann krank, wenn er sich nicht kontrollieren lässt und unerwartet auftritt. Experimente lassen sich zum Beispiel so konstruieren, dass eine Maus bei Auseinandersetzungen immer verliert. Experten sprechen von „social defeat“ – „sozialer Niederlage“. Eine solche Maus entwickelt zwar keine Depression, zeigt aber krankhafte Veränderungen. So kann sie zum Beispiel apathisch oder fettleibig werden. Diese Ergebnisse seien auf den Menschen übertragbar, betont Schmidt: „Auch beim Menschen wirkt vor allem jener Stress besonders stark, der unkontrollierbar und unberechenbar ist, zum Beispiel bei Mobbing, das Menschen auf Dauer krank machen kann.“ Ein anderes Beispiel sei die Corona-Pandemie gewesen. Zu Beginn der Pandemie im Frühjahr 2020 war noch unklar, wie gefährlich der Erreger ist und wie man sich wirkungsvoll dagegen schützen kann. Die Menschen fühlten sich ständig einer unberechenbaren Gefahr ausgesetzt. „Durch diesen chronischen Stress hat die Zahl depressiver Symptome damals messbar zugenommen“, erklärt der Max-Planck-Forscher (Abb. B). Als dann die ersten Impfstoffe auf den Markt kamen und klar wurde, wie man sich schützen kann, nahm der Stress wieder ab. „Kontrollierbaren Stress können wir Menschen deutlich besser bewältigen.“ Prüfungsstress kann man beispielsweise minimieren, indem man frühzeitig beginnt, den Lernstoff in kleine Einheiten aufteilt und einen Zeitplan erstellt. Durch Simulieren der Prüfungssituation gewinnt man an Sicherheit. Zu bedenken ist aber auch, dass jeder Mensch anders auf Stressoren reagiert“, so der Wissenschaftler.
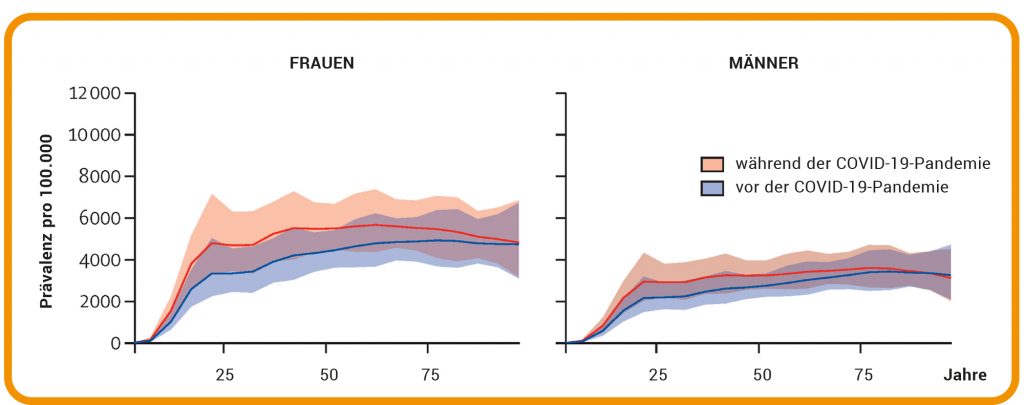
Abb. B: Mögliche Folgen von unkontrollierbarem Stress. Globale Prävalenz von schweren depressiven Störungen vor und während der COVID-19-Pandemie nach Alter und Geschlecht.
© Quelle: Lancet 2021; 398: 1700–12, Fig. 1 (Auszug); https://doi.org/ 10.1016/S0140-6736(21)02143-7 / CC BY 4.0
Anhaltender, unkontrollierbarer Stress und traumatische „Stresserlebnisse“ können also zu einer Depression führen. Welche Mechanismen dahinterstecken und welche Veränderungen im Stoffwechsel Depressionen auslösen, hat man bisher aber nur zum Teil verstanden. Vor 50 Jahren gingen Fachleute noch davon aus, dass Depressionen einzelne, klare Auslöser hätten. Gemäß dieser Vorstellung habe die Erkrankung ihre Ursache in veränderten biochemischen „Pfaden“ (engl. pathways), also einzelnen, klar umrissenen Stoffwechselwegen. Inzwischen ist die Forschung deutlich weiter: Tatsächlich können Depressionen viele verschiedene biologische Auslöser haben. Etwa ein Drittel des Risikos, an einer Depression zu erkranken, ist auch genetisch bedingt – Genomanalysen von Menschen mit Depressionen haben gezeigt, dass viele Gene an der Entstehung einer Depression beteiligt sind. Dieses genetische Risiko spielt mit den Risiken durch Stress zusammen, und könnte zum Teil erklären, warum Menschen resilient oder weniger resilient gegenüber Stresserfahrungen sind.
Ein Forschungsteam am Max-Planck-Institut für Psychiatrie ist genau dieser Frage nachgegangen, welche genetischen Varianten an der Reaktion auf Stress und dem Risiko, eine psychiatrische Störung zu entwickeln, beteiligt sein könnten. Dazu nutzten sie eine Substanz namens Dexamethason, die ähnlich wirkt wie das Stresshormon Cortisol und ebenso wie dieses eine molekulare und zelluläre Antwort, beginnend auf der Ebene der DNA, auslöst. Das Team untersuchte Zellen, die besonders empfindlich auf Stress reagieren. Dabei fanden sie über 500 Stellen im Erbgut (sog. Loci), die Reaktionen auf Stress zeigten, sowie 79 genetische Varianten, die die Expression von Genen und somit die molekulare Antwort auf Stress nur bei Behandlung mit Dexamethason beeinflussten. Diese Varianten stehen, wie große internationale Studien gezeigt haben, auch im Zusammenhang mit dem Risiko, eine psychiatrische Störung zu entwickeln.
Um herauszufinden, wie die Kombination der Varianten dieses Risiko beeinflusst, unterzog das Forschungsteam die Teilnehmenden der Studie einer Stressaufgabe. Dabei zeigte sich, dass eine höhere Anzahl dieser „stressreaktiven“ Genvarianten mit einem Anstieg des Cortisolspiegels bei den entsprechenden Probanden verbunden war. Dieser Unterschied wurde vor der Stressaufgabe nicht beobachtet, was heißt, dass diese Varianten nur in Stresssituationen von Bedeutung waren. Personen mit vielen dieser Genvarianten konnten ihr Stresshormon-System nach der Aufgabe nicht wieder schnell normalisieren und waren dadurch „unnötig“ lange gestresst. So zeigte ein weiterer Test, dass Personen mit mehr Risikovarianten bei Erschrecken intensiver reagierten und sich die Stärke der Schreckreaktion auch nach Wiederholen des Schreckreizes noch erhöhte. „Dabei hätte man eigentlich ein verringerte Reaktionen durch Gewöhnung erwartet“, erklärt Elisabeth Binder, Direktorin am Max-Planck-Institut für Psychiatrie.
„Die Genetik hat also einen Einfluss auf die Empfindlichkeit unserer Reaktion auf Stress. Der molekulare Mechanismus könnte erklären, warum belastende Lebensereignisse mal mehr oder weniger mit psychiatrischen Störungen korrelieren“, fasst Binder die Ergebnisse zusammen. Diese Erkenntnisse seien wichtig für die Vorhersage, welche Menschen ein höheres Risiko haben, als Reaktion auf Stress psychiatrische Störungen zu entwickeln, so die Forscherin weiter. Das könnte helfen, frühzeitig Hilfen anzubieten, um die Entwicklung von psychiatrischen Störungen zu vermeiden.
In zahlreichen Forschungsprojekten wird nach neuen Therapieansätzen für psychiatrische Störungen gesucht. Im Fokus der Untersuchungen steht dabei jenes Stresshormon-System, das unsere Anpassung an Stresssituationen koordiniert, die sogenannte Hypothalamus-Hypophysen-Nebennieren-Achse (HPA-Achse). Eine wichtige Schaltstelle in diesem System ist der Glukokortikoid- Rezeptor. Er kommt in nahezu allen Zellen vor und reguliert dort die Genexpression. Aber erst wenn das Stresshormon Cortisol an den Rezeptor bindet, kann dieser an die entsprechenden Kontrollstellen auf der DNA binden (Abb. C) und so die Transkription und damit die Biosynthese vieler verschiedener Proteine anstoßen, die für die Stressreaktion wichtig sind.
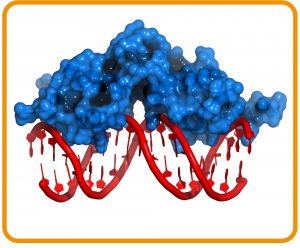
Abb. C: Schaltstelle für Stress. Glucocorticoid-Rezeptor (DNA-Bindungsdomäne), gebunden an einen DNA-Doppelstrang.
© molekuul.be / Adobe Stock
Die Empfindlichkeit des Glukokortikoid-Rezeptors gegenüber Cortisol wird durch eine Reihe von Molekülen, sogenannte Chaperone und Co-Chaperone moduliert. Chaperone beeinflussen die Aktivität anderer Proteine, indem sie diese bei der Faltung in ihre dreidimensionale Struktur unterstützen. Sie sind in verschiedenen Zelltypen und bei verschiedenen Proteinen aktiv. Das Chaperon mit dem Kürzel FKBP51 ist von besonderem Interesse, denn es setzt die Cortisol-Bindefähigkeit des Glukokortikoid-Rezeptors herab. Auf diese Weise sorgt es dafür, dass die Stressreaktion des Körpers wieder heruntergefahren wird, wenn der äußere Stress nachlässt, eine bedrohliche Situation beispielsweise vorüber ist. Das ist ein ganz natürlicher und wichtiger Mechanismus. Genomanalysen bei Menschen mit Stress-bedingten psychiatrischen Erkrankungen, wie der posttraumatischen Belastungsstörung (PTBS) und Depressionen, haben gezeigt, dass bei manchen von ihnen Veränderungen an genau jenem Gen vorliegen, das für das Chaperon FKBP51 kodiert. Möglicherweise wird FKBP51 deshalb vermehrt synthetisiert und dämpft den Glukokortikoid-Rezeptor dauerhaft. Das könnte, so die Annahme, bei depressiven Menschen zu Antriebslosigkeit und Niedergeschlagenheit führen. Auch Veränderungen der Interaktionen des Chaperons mit anderen für Nervenzellen wichtigen Proteinen könnten eine Erklärung dafür sein, warum manche Menschen mehr oder weniger stressresistent sind.
Chaperone sind ein hochinteressanter, potenzieller Angriffspunkt (engl. target) für neue Medikamente und damit verbunden die Therapie depressiver Menschen. Derzeit werden erste Chaperon-Antagonisten entwickelt, die die Aktivität der Chaperone oder deren Biosynthese hemmen. Die Herausforderung dabei: Es gibt viele verschiedene Chaperone, die in ganz verschiedenen Zellen und Geweben aktiv sind und die ganz unterschiedliche Stoffwechselreaktionen steuern. Das bedeutet, dass Chaperon-Antagonisten im Körper sehr gezielt in die für die Stressreaktion zuständigen Zellen eingeschleust werden müssten. Wie sich eine solche gezielte Form des „drug delivery“ technisch umsetzen ließe, ist noch Gegenstand der Forschung.
Aber es sind nicht immer die Gene, die dazu führen, dass manche Menschen nach einem traumatischen Erlebnis eine Depression entwickeln, während andere Menschen mit gleicher Erfahrung nicht erkranken. Tatsächlich spielen auch epigenetische Prozesse eine zentrale Rolle: Sie verändern beispielsweise das Muster der Methylgruppen an der DNA und damit die Aktivierbarkeit bestimmter Gene in bestimmten Zellen oder Organen (s. Biomax 23). So prägt die Epigenetik auch unser Stresssystem. Frühkindlicher Stress beispielsweise kann sich langfristig auf die psychische Gesundheit auswirken und das Risiko für die Entwicklung von Angststörungen und einer posttraumatischen Belastungsstörung erhöhen.
„Stress und Trauma in der Kindheit sind ein maßgeblicher Risikofaktor“, betont Elisabeth Binder. So gehen belastende Kindheitserfahrungen mit einem doppelt so hohen Risiko für depressive Störungen und einem 2,7-fach erhöhten Risiko für Angststörungen im Erwachsenenalter einher. Aber: „Ganz ohne Stress kann auch keine Resistenz aufgebaut werden“, betont die Medizinerin. Tatsächlich legt die Stressforschung der vergangenen Jahre nahe, dass Stressresistenz in der frühkindlichen Entwicklung erlernt wird. Durch seine Experimente an Mäusen hat Mathias V. Schmidt herausgefunden, dass es offenbar wichtig ist, in der Kindheit moderaten Stress zu erfahren. „Stresserfahrung ist essenziell, damit die Mäuse „lernen“, mit Stress umzugehen“, sagt Schmidt. Das sei höchstwahrscheinlich auch beim Menschen so. „Wer zum Beispiel überbehütet aufwächst, kann später den Stress, den Konflikte zwangsläufig mit sich bringen, schlechter bewältigen“, so der Forscher.
Dieses „Stress-Lernen“ findet sehr wahrscheinlich ebenfalls zu einem Teil auf der epigenetischen Ebene statt. „Wir gehen heute davon aus, dass das Erlernen von Stress in der frühkindlichen Entwicklung durch die Methylierung gesteuert wird“, sagt der Max-Planck-Forscher. Epigenetische Veränderungen fänden auch an den Histonen statt, jenen Proteinen, um die der DNA-Strang im Zellkern gewickelt ist. Durch Acetylierung der Histone kann die Wicklung verfestigt oder gelockert werden. Auch das beeinflusst, ob bestimmte Gene aktiviert oder unterdrückt werden. Mittlerweile gibt es konkrete Hinweise darauf, dass zahlreiche epigenetische Veränderungen einen Einfluss darauf haben, wie verschiedene Menschen auf Stress reagieren.
Um die Entwicklung psychiatrischer Erkrankungen zu verstehen, müssen somit neben den genetischen Analysen auch die epigenetischen Kodierungen identifiziert werden. Damit tun sich viele neue Wege für Therapien auf. Stress und Depressionen mögen ein komplexes Phänomen sein, doch die jüngsten Erkenntnisse liefern auch viele Ansatzpunkte für neue Medikamente. Schmidt: „Diese Entwicklungen stimmen mich zuversichtlich, dass wir in den nächsten Jahren große Fortschritte beim Verständnis des Stresses und bei der Entwicklung neuer Wirkstoffe gegen Depressionen und andere psychische Erkrankungen machen werden.“
Schau mir in die Augen – Pupillometrie als Diagnoseergänzung
Antriebslosigkeit ist eines der meist beobachteten Symptome der Depression. Ein Forscherteam des Max-Planck-Instituts für Psychiatrie hat herausgefunden, dass die geringere Pupillenreaktion bei Patienten und Patientinnen einen entsprechenden Hinweis darauf liefert. Bei gesunden Menschen erweitern sich die Pupillen bei der Erwartung auf eine Belohnung, wohingegen diese Reaktion bei Personen mit Depressionen weniger aus geprägt ist. Die Pupillenreaktion ist unter anderem ein Marker für die Aktivität im Locus Coeruleus, einer Gehirnstruktur mit der größten Ansammlung noradrenerger Neuronen im zentralen Nervensystem. Sie könnte als ergänzende Methode zur Diagnosestellung eingesetzt werden. Wenn beispielsweise ein Patient starke Beeinträchtigungen in der Pupillenreaktion zeigt, könnten Antidepressiva, die auf das noradrenerge System wirken, effektiver als andere Medikamente sein.
Abbildungshinweise:
Titelbild: © HNBM
Abb. A: © Quelle Zahlen: Techniker Krankenkasse (TK-Stressstudie, 2021); Grafik: HNBM
Abb. B: © Quelle: Lancet 2021; 398: 1700–12, Fig. 1 (Auszug); https://doi.org/ 10.1016/S0140-6736(21)02143-7 / CC BY 4.0
Abb. C: © molekuul.be / Adobe Stock
Abb. im Kasten: © MPI für Psychiatrie
Der Text wird unter CC BY-NC-SA 4.0 veröffentlicht.
BIOMAX Ausgabe 40, April 2025; Text: Christina Beck, Tim Schröder; Redaktion: Tanja Fendt

Foto: © Giovanni Cancemi / Adobe Stock
In der Folge erklärt die Neurowissenschaftlerin Dr. Anne Schäfer vom Max-Planck-Institut für Biologie des Alterns, wie Neuronen altern und welchen Einfluss dabei Lebensstil und Infektionskrankheiten haben.
Inhalte:
Gliazellen, Neuronen, Alzheimer-Erkrankung, Einfluss Lebensstil, Myelinschicht, neuronale Stammzellen, Plaques, Gemeinsamkeiten und Verbindung von Immun- und Nervensystem bei Infekten, Mikrogliazellen
Kapitel:
min 01:40: Woran erkennt man das Alter des Gehirns?
min 03:44: Was passiert beim Altern auf neuronaler Ebene?
min 05:37: Zusammenfassung: Zusammenarbeit Neuronen und Gliazellen
min 07:23: Einfluss des Lebensstils auf Alterungsprozesse im Gehirn
min 09:00: Einfluss Denksportaufgaben
min 10:04: Zusammenfassung: Auswirkung von Lebensstil, Training des Gehirns
min 11:27: Einfluss von Infektionen
min 16:02: Beispiele für neuronale Veränderungen bei Infekten
min 16:50: Ist eine Manipulation der Mikrogliazellen möglich?
Zum Podcast (20 min) vom 20. November 2023 © detektor.fm / Max-Planck-Gesellschaft
Schokoriegel, Chips und Pommes – warum können wir sie im Supermarkt nicht einfach links liegen lassen? Forschende des Max-Planck-Instituts für Stoffwechselforschung in Köln haben, in Zusammenarbeit mit der Yale University, jetzt nachgewiesen, dass Lebensmittel mit hohem Fett- und Zuckergehalt unser Gehirn verändern: Wenn wir regelmäßig auch nur kleine Mengen davon essen, lernt das Gehirn, auch weiterhin genau diese Lebensmittel konsumieren zu wollen. „Unsere Messungen der Gehirnaktivitäten haben gezeigt, dass sich das Gehirn durch den Konsum von Pommes und Co. neu verdrahtet. Es lernt unterbewusst belohnendes Essen zu bevorzugen. Durch diese Veränderungen im Gehirn werden wir unbewusst immer die Lebensmittel bevorzugen, die viel Fett und Zucker enthalten“, sagt Marc Tittgemeyer, der die Studie leitete.
Im Kurzfilm (2 min) erklärt Cedric Engels die Erkenntnisse aus der Forschung.
Weitere Infos im Artikel der MaxPlanckForschung 1/2023 (>PDF)
Das passende BIOMAX-Heft zum Thema Synapsen erklärt die Vorgänge in Nervenzellen, die grundlegend für Lernprozesse sind.
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
YouTube-Link: https://youtu.be/5LWZm4bJOBA
[Dauer des Videos: 1:30 min]
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
YouTube-Link: https://youtu.be/deY2N5NMFFk
Ein Vortrag von Prof. Dr. Simone Kühn, Max-Planck-Institut für Bildungsforschung, Berlin, Leiterin der Lise-Meitner-Gruppe für Umweltneurowissenschaften
[Dauer des Vortrags: ca. 20 min]
Themen im Vortrag: Forschungsmethoden (z.B. funktionelles MRT) / neuronale Plastizität / Einfluss der Umwelt (Stadt/Land) auf das Verhalten und Gehirnstrukturen (z.B. Amygdala, Hippocampus, präfrontaler Cortex) / Effekte extremer Umwelten
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
YouTube-Link: https://youtu.be/byaYYglUjhM
Angst ist durchaus ein sinnvolles, ja lebenswichtiges Gefühl, denn es löst ein entsprechendes Schutzverhalten aus. Wenn die Angst vor bestimmten Objekten oder Situationen aber überhandnimmt, dann kann sie zur Gefahr für die eigene Gesundheit werden. Krankhafte Angst liegt dann vor, wenn Menschen bei Ängsten nicht in der Lage sind, ihre Gedanken und Gefühle kontrollieren zu können. So empfinden manche Menschen zum Beispiel übertriebene Angst beim Anblick von Spritzen und lassen sich deshalb nicht impfen. Wird Angst übermächtig, sprechen Forscherinnen und Forscher von einer Phobie. Aber was ist das eigentlich genau? Ab wann entwickelt sich Angst zu einer krankhaften Angststörung? Was kann man dagegen tun? Und – was hat das alles mit Virtual Reality zu tun? Das wollen wir uns in diesem Video genauer anschauen.
[Dauer des Videos: 17 min]
Themen im Video: Evolutionäre Vorteile von Angst / Definition Phobie / Entstehung von Angst (Gehirnregionen) / Messung von Angst (Methoden) / Behandlung von Phobien
Datenschutzhinweis: Mit dem Klick auf den Play-Button starten Sie ein YouTube-Video. Vorher werden keine Daten an YouTube übertragen.
Die Aufgaben behandeln folgende Themen:
Informationsübertragung an der chemischen Synapse / Alzheimer / Kurzzeitplastizität / Munc-13 / Verstärkung von Synapsen
Unterrichtsmaterial zum Biomax 22.
Die Aufgaben beziehen sich auf eine Animation zu Vorgängen im Kaliumkanal. Die Schülerinnen und Schüler sollen die Vorgänge in der Animation beschreiben, erklären und einen Text dazu verfassen.
Unterrichtsmaterial zum Biomax 15.
Zehn Filme zu den Forschungsthemen aus Biologie, Physik und Geographie bietet die zweite MaxPlanckCinema-DVD.
Alle Filme sind auch einzeln in max-media zu finden.
Inhalte:
Biologie: Evolution; Zellorganellen; Proteinfaltung; Epigenetik
Physik / Chemie: STED-Mikroskopie; Brennstoffzellen; Gehirn-Computer-Schnittstelle; Gammablitze; Exoplaneten
Geographie: Wolken
Die DVD umfasst 19 Filme von jeweils 6 bis 9 Minuten, die acht verschiedene Themenkomplexe aus Biologie, Physik und Geographie abdecken. Zu jedem Thema gehören ein 3D-animierter Grundlagenfilm sowie ein Einstiegsfilm, der mit Unterstützung von Comic-ähnlichen Sequenzen in die aktuelle Forschung einführt.
Alle Filme sind auch einzeln in max-media zu finden.
Inhalte:
Biologie: Synaptische Platizität; Riechen; Proteomik; Pflanzliche Abwehr
Physik: Laser; Die Sonne; Gravitation
Geographie: Klimamodelle