Techmax 28: Nachwachsende Nanowelt
Cellulose-Kristalle werden zum grünen Zukunftsmaterial
Die Nanowelt hat ganz eigene, manchmal magisch anmutende Gesetze. Der Name kommt vom altgriechischen Wort nános für Zwerg. Nanoobjekte bemessen sich in Milliardstel Metern, Nanometer genannt. Die kleinsten von ihnen sind grob zehnmal größer als Atome. Die größten messen bis zu hundert Nanometer. Auf der Rangfolge der Größenskalen liegt die Nanowelt also oberhalb der Atome, aber unterhalb der Mikrowelt. Dort ist der Mikrometer, als ein Millionstel Meter, das passende Maß (Abb. A).
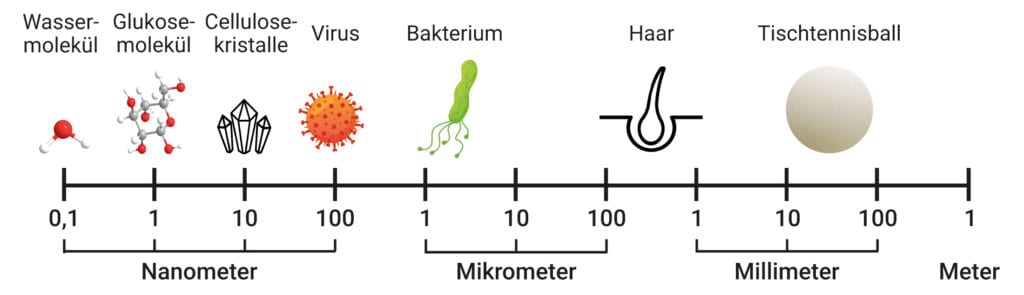
Abb. A: Die Nanowelt reicht ungefähr von einem bis 100 Nanometer. Die gezeigten Beispiele sind nach der Größe ihres Querschnitts einsortiert.
© R. Wengenmayr; MPG
In der Natur gibt es viele Nanopartikel, etwa kleine Viren oder Antikörper im Blut. Zudem setzen wir Menschen immer mehr künstliche Nanopartikel frei, zum Beispiel in Imprägniersprays oder Kosmetika. Silbernanopartikel werden in medizinischen Wundauflagen benutzt, weil sie Keime abtöten. In der Nanowelt regiert vor allem ein Gesetz, das aus der Geometrie stammt: Je kleiner zum Beispiel eine Kugel ist, desto größer ist ihre Oberfläche im Verhältnis zum Volumen. Deshalb besitzen Nanopartikel eine verhältnismäßig riesige Oberfläche. Diese bietet der Chemie eine große Spielwiese für Reaktionen, die auf verschiedenen Wechselwirkungen basieren. Zum Beispiel können Nanopartikel aus Eisen so heftig mit Luftsauerstoff oxidieren, dass sie von selbst in Flammen aufgehen. Auch als Katalysatoren, die auf ihrer Oberfläche Reaktionen beschleunigen, eignen sich Nanopartikel besonders gut. Dank ihrer Eigenschaften kann die Nanowelt eine Vielfalt neuer Anwendungen hervorbringen. Nanopartikel können wegen ihrer Reaktionsfreudigkeit aber auch zum gesundheitlichen Risiko werden. Diese Sorge wächst mit der Menge an künstlich freigesetzten Nanopartikeln. Genau hier setzt das Forschungsgebiet von Svitlana Filonenko an. Die Chemikerin leitet eine Gruppe am Max-Planck-Institut für Kolloid- und Grenzflächenforschung in Potsdam, in der Abteilung des Direktors Markus Antonietti. Ihr Forschungsgebiet ist Nanocellulose, die umweltverträglich und vielfältig einsetzbar ist.
Nachhaltige Cellulose für grüne Chemie
„Cellulose ist eines der häufigsten organischen Polymere auf unserem Planeten“, sagt Filonenko: „Und dieser Rohstoff wächst jedes Jahr nach!“ Schon ist sie bei der „grünen Chemie“ gelandet. Grüne Chemie soll umweltfreundliche Verfahren einsetzen, nachhaltige Rohstoffe verwenden und biologisch abbaubare Produkte hervorbringen. Dafür ist Cellulose ideal. Cellulose begegnet uns im Alltag in vielfältiger Form, als Holz, Karton, Papier, Filter oder Kleiderstoffe aus Baumwolle und Viskose. Und wir essen sie, als Gemüse, Obst, Salat, aber auch in Form von lebensmittelchemischen Zusatzstoffen, etwa Verdickungsmittel. Produziert wird Cellulose vor allem von Pflanzenzellen, aber auch von einigen Bakterien und sogar Tieren – die Manteltiere, zu denen die Seescheiden gehören. Wie viele Naturmaterialien sind Pflanzenfasern komplex aufgebaut, die eigentliche Cellulose aber überraschend einfach. Ihr Grundbaustein ist das Traubenzucker-Molekül, die Glucose. Pflanzen produzieren es in der Fotosynthese mit Hilfe von Sonnenlicht aus Wasser und Kohlenstoffdioxid. Die Pflanzenzelle verknüpft die Glucose-Moleküle unter Einsatz eines Enzyms zu einer Polymerkette (Abb. B).
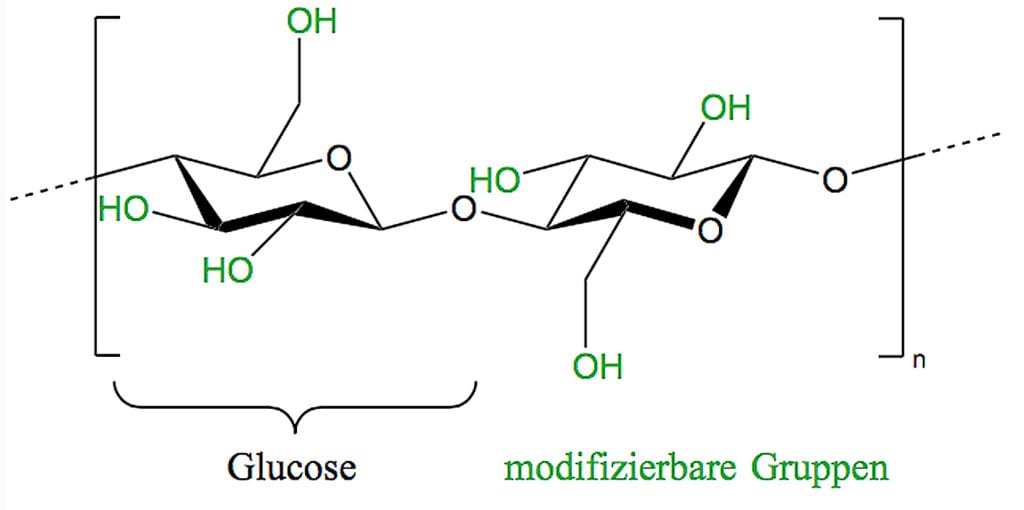
Abb. B: Cellulose ist wie eine Perlenkette aus einzelnen Bausteinen (Glucosemoleküle) aufgebaut, die sich immer wiederholen. Zwei Glucosemoleküle, die gegeneinander verdreht aneinandergeknüpft sind, bilden die kleinste Einheit des Polymers. Die grün gefärbten OH-Gruppen lassen sich chemisch modifizieren.
© E. Jaekel, MPI für Kolloid- und Grenzflächenforschung / CC BY-NC-ND 4.0
„Die Zelle produziert viele solcher Polymerketten gleichzeitig“, erklärt Filonenko. Daraus entsteht dann das eigentliche Forschungs-objekt der Chemikerin. Die Polymerketten werden schön ordentlich zu einem Kristall zusammengefügt. Kristalle zeichnen sich durch eine nahezu perfekte, dreidimensionale Anordnung ihrer Grundbausteine aus. Eigentlich sind Kristalle typisch für unbelebte Materie, doch auch lebende Organismen können welche herstellen. Allerdings sind Kristalle hart und oft spröde. Wie kann daraus eine biegsame, zähe Pflanzenfaser entstehen? Das verdankt sie einem Zusammenspiel mit weiteren Bestandteilen. Nachdem die Zelle den Cellulose-Kristall bis zu einer bestimmten Länge gebaut hat, fängt sie an, Fehler zu machen. „Diese Abschnitte sind amorph“, erklärt Filonenko. Amorph ist das Gegenteil kristalliner Ordnung. Wie in einer Perlenkette wechseln sich kristalline mit amorphen Abschnitten ab. In Letzteren können sich die Polymere gegeneinander verschieben, was die Fasern biegsam macht. Sie sind für Filonenkos Forschung auch wichtig, weil sich hier die Cellulose-Kristalle chemisch heraustrennen lassen.
Damit ist die Pflanzenfaser noch nicht fertig. Jetzt kommt ein anderes Biopolymer dazu: Lignin macht die Faser wasserfest. Reine Cellulose ist nämlich stark wasseranziehend, also hydrophil. Lignin hingegen ist wasserabweisend, hydrophob, und umhüllt das Cellulosepolymer. Außerdem sorgt das harte Lignin für die nötige Druckfestigkeit der Pflanzenzellwand. Allerdings lassen sich die wasserliebende Cellulose und das fettliebende Lignin nur schwer chemisch „verheiraten“. Dies übernimmt das dritte Element der Pflanzenzellwand, die Hemicellulose. Sie lagert sich um die Cellulosefibrille herum an und ermöglicht das Einbetten der Cellulosefaser in Lignin. Aber immer noch ist die Pflanzenfaser nicht fertig. Die eingebetteten Mikrofasern werden von der Pflanzenzelle nochmals zu einer Makrofaser gebündelt. Und mehrere Makrofasern bilden eine fertige Pflanzenfaser (Abb. C).
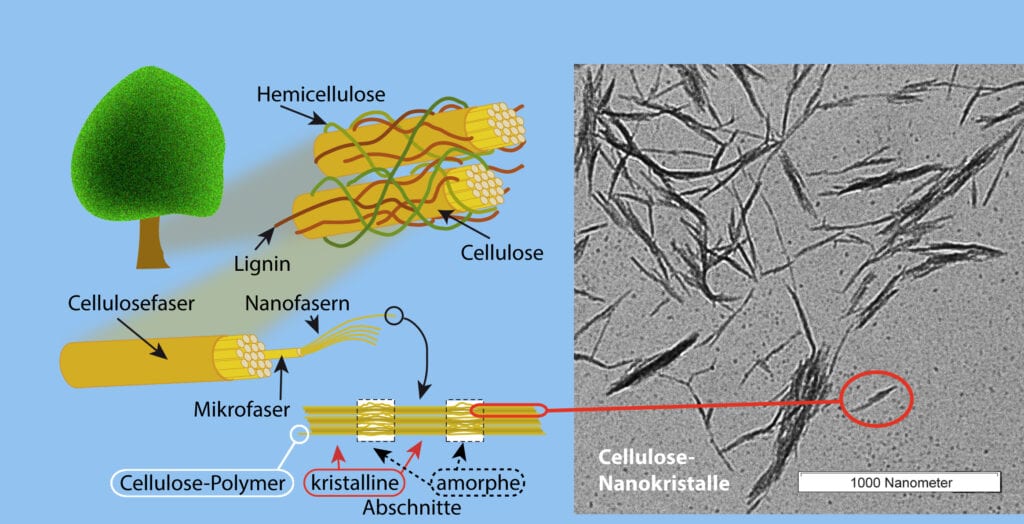
Linkes Bild C1: Pflanzenfaser (rechts oben), Cellulosefaser und deren Aufbau bis zum Cellulose-Nanokristall.
Rechtes Bild C2: Die rot eingekreiste Struktur ist ein ungefähr 200 nm langer Cellulose-Nanokristall.
C1: © R. Wengenmayr / CC BY-NC-SA 4.0 C2: © MPI für Kolloid- und Grenzflächenforschung / CC BY-NC-ND 4.0
Nanowelt trifft auf Mikrowelt
„Die Cellulose-Kristalle sind ungefähr fünf bis zwanzig Nanometer dick und können bis zu 300 Nanometer lang sein“, erklärt Svitlana Filonenko. Die genauen Maße hängen vom erzeugenden Organismus ab. Damit gehören diese Kristallnadeln im Quer-schnitt zur Nanowelt, in ihrer Länge dagegen schon zur Mikrowelt. Die langgestreckte Form der Cellulose-Nanokristalle sorgt für faszinierende Eigenschaften. Mechanisch sind sie enorm stabil, vergleichbar mit Stahl, haben Experimente gezeigt. Auf ihrer Oberfläche konzentriert sich elektrische Ladung. Damit ziehen sie Wassermoleküle stark an, denn diese Moleküle haben bei den Wasserstoffatomen einen positiven, beim Sauerstoff einen negativen elektrischen Pol. Das macht die Cellulose enorm hydrophil. „Schon ein Anteil von nur zwei Prozent Nanocellulose in Wasser erzeugt ein sogenanntes Hydrogel“, sagt Filonenko (Abb. D).

Abb. D: Dieses Hydrogel besteht aus 98 Prozent Wasser und zwei Prozent Cellulose-Nanokristallen.
© Dr. Nieves Lopez Salas
Die langen Kristallnadeln bilden ein sehr lockeres Netzwerk, in dessen Lücken sich viel Wasser ansammelt. Dieser extreme Wasseranteil ist zum Beispiel interessant für biologisch abbaubare Kosmetika, an denen die Chemikerin forscht. „Mehr Feuchtigkeit in einer Creme geht nicht“, sagt sie lachend. Kosmetika benötigen allerdings auch einen Fettanteil. Wasser und Öl sind aber nicht mischbar. Für den Mix müssen normalerweise Emulgatoren sorgen. Das sind Moleküle, die einen wasser- und einen fettliebenden, also lipophilen, Teil haben. Damit können sie Wasser und Öl zu einer Emulsion verbinden.
Sogenannte Pickering-Emulsionen kommen ohne klassische Emulgatoren aus. Hier sorgen allein feine, feste Partikel für die Verbindung zwischen Wasser und Öl. Mit Cellulose-Nanokristallen funktioniert das sehr gut. Zum Glück befinden sich auf den langen Nanokristallen auch Abschnitte ohne elektrische Ladung, erklärt Filonenko. Hier können die Moleküle von Fetten und Ölen andocken. Die Potsdamer Chemikerinnen versuchen zusätzlich, die Cellulose-Nanokristalle an der Oberfläche chemisch zu optimieren. Das soll für eine stabilere Verbindung zwischen Öl und Wasser sorgen. Mit solchen Pickering-Emulsionen ließen sich umweltfreundliche, biologisch abbaubare Kosmetika herstellen. Das ist ein wichtiges Thema, da heute täglich Kosmetika-Rückstände von Milliarden von Menschen in die Umwelt gelangen.
Biologisch abbaubare Lebensmittelverpackungen
Ein anderes Forschungsgebiet der Potsdamer sind Verdickungsmittel für Lebensmittel. Die Nanocellulose verspricht, besser verträglich als manche heute eingesetzten Lebensmittelzusatzstoffe zu sein. Doch auch die Papierverpackungen von Lebensmitteln hat Filonenko im Blick: „Ich denke an die jüngsten Skandale um Spuren von Mineralöl in Lebensmitteln.“ Das Problem erwächst hier sogar aus der Nachhaltigkeit, denn die Verpackungen werden aus Altpapier gemacht. Das kommt aus vielen Quellen und kann verschmutzt sein. Um die Lebensmittel zu schützen, werden die Verpackungen daher innen mit einer Kunststoffschicht abgedichtet. Die ist aber nicht biologisch abbaubar. Filonenkos Team will bei dieser Beschichtung den Kunststoff durch Cellulose-Nanokristalle ersetzen. Nach dem Aufbringen einer Flüssigkeit legen sich beim Trocknen die langen Kristallnadeln dicht geordnet aneinander. Die Lücken zwischen ihnen sind zu klein, um noch unerwünschte Stoffe durchzulassen. Diese Schichten sind zudem ein Augenschmaus. „Sie schillern in allen Regenbogenfarben“, sagt die Chemikerin begeistert. Der Grund: Die Kristallnadeln sortieren sich zu in sich verschraubten Helixstrukturen, und diese Mikrostrukturen brechen das Licht in unterschiedlichen Farben, je nach dem, aus welchem Winkel man sie anschaut. Es ist derselbe physikalische Effekt, der Schmetterlingsflügel schillern lässt.
Filonenko ist von Cellulose-Nanokristalle auch begeistert, weil jeder Glucose-Baustein drei funktionelle Gruppen besitzt (grün in Abb. B): „An diese drei Zentren kann man verschiedene Moleküle binden, um die Cellulose-Nanokristalle zu modifizieren.“ Trotz dieser chemischen Flexibilität ist die Gewinnung der Nanokristalle bislang eine harte Nuss. Die Cellulosefasern, in denen sie stecken, sind weder in Wasser noch in organischen Lösungsmitteln löslich. Ohne Lösung sind aber chemische Reaktionen schwierig. Daher zerlegt das heute etablierte Verfahren die Fasern in Schwefelsäure, um die Nanokristalle herauszutrennen. Hydrolyse heißt die Prozedur. Schwefelsäure ist aber stark ätzend und gefährlich handzuhaben. Grüne Chemie will sie daher vermeiden, und Filonenkos Team forscht an einer schonenderen Methode für die Zukunft.
Eutektische Flüssigkeiten
Das Zauberwort heißt „stark eutektische Lösungsmittel“. Damit lassen sich die Nanokristalle vergleichsweise sanft aus den Cellulosefasern herauslösen. Zuerst muss Filonenko erklären, was ein Eutektikum ist: „Wenn man zwei oder mehr feste Komponenten mit bestimmten Eigenschaften mixt, sinkt die gemeinsame Schmelztemperatur auf einen Tiefpunkt, das Eutektikum.“ Sie verdeutlicht das Prinzip an einem Beispiel, mit dem sie kürzlich eine kanadische Chemieprofessorin verblüfft hat: Ahornsirup ist ein natürliches eutektisches Gemisch. Die zwei Hauptbestandteile des Sirups sind Äpfelsäure und Zucker, genauer Saccharose und Fructose. Bei Zimmertemperatur sind alles feste Substanzen. Man mischt sie als Pulver und träufelt ein wenig Wasser darauf, um die Komponenten in Kontakt zu bringen. „Jetzt geschieht etwas Faszinierendes“, erklärt die Chemikerin: „Das Pulver wird immer feuchter, bis es sich in eine klare Flüssigkeit verwandelt.“ Das Wasser wirkt hier nicht als Lösungsmittel, denn davon gibt es viel zu wenig, um die Pulver aufzulösen. Stattdessen ist die Flüssigkeit eine Schmelze bei Zimmertemperatur.
Eine solche eutektische Flüssigkeit kann ein sehr gutes Lösungsmittel für bestimmte Stoffe sein. Dazu gehört die Cellulose, für die Filonenkos Team ein eutektisches Lösungsmittel entwickelt hat. Die Chemie ist allerdings komplizierter als beim Ahornsirup. Das Team kann auch noch keine Details verraten, weil die Arbeit erst in einem wissenschaftlichen Fachblatt publiziert werden muss. Esther Jaekel, eine Doktorandin in Filonenkos Gruppe, führt aber im Labor vor, was damit passiert. Als Rohmaterial testet sie gerade verschiedene cellulosehaltige Abfälle, darunter Faserreste aus der Papierproduktion, sogar Holzspäne. Je bräunlicher das Material ist, desto mehr Lignin und Hemicellulose enthält es. Zum Herauslösen der Nanokristalle wird es mit einer klaren, wässrigen Flüssigkeit gemischt. Das ist das bereits fertige eutektische Lösungsmittel aus zwei Komponenten. Es zersetzt die amorphen Verbindungen zwischen Cellulose-Kristallen, nur die Nanokristalle bleiben übrig.
In einigen Experimenten soll das eutektische Lösungsmittel die Cellulose-Nanokristalle modifizieren. Das passiert in einem kleinen Reaktor, der wie ein robuster Schnellkochtopf funktioniert. Darin wird die Mischung zum Beispiel bei 140 Grad Celsius und dem fünfzigfachen Atmosphärendruck für eine Stunde „gegart“. In dieser Zeit läuft die erwünschte Veränderung ab. Hinterher bekommen die Chemikerinnen eine bräunliche Flüssigkeit, wobei die braune Farbe durch Röststoffe wie beim Braten entsteht. Diese werden anschließend herausgewaschen. Das Ergebnis ist eine milchige Flüssigkeit, die ausschließlich fein verteilte Cellulose-Nanokristalle enthält. „Das ist ein stabiles Kolloid“, erklärt Jaekel, und damit kommt noch ein wichtiges Fachwort ins Spiel. Das Wort Kolloid leitet sich aus dem Altgriechischem ab und bedeutet so viel wie „leimartiges Aussehen“. Die Kolloidchemie, der sich Markus Antoniettis Abteilung im Institut widmet, basiert auf Nanopartikeln in Flüssigkeiten. Solche extrem feine Partikel setzen sich nicht mehr unten im Gefäß ab, wenn die Flüssigkeit länger steht. Die Wärmebewegung der Moleküle kickt die kleinen Partikel immer zurück in die Flüssigkeit.
Aus dem Nanocellulose-Kolloid lässt sich zum Beispiel eine Pickering-Emulsion machen. Jaekel zeigt ein Fläschchen mit einer milchig-weißen Flüssigkeit: „Das ist eine Emulsion von Öl in Wasser, also im Prinzip Salatsauce.“ Die Chemikerinnen gefriertrocknen auch die gewonnene Flüssigkeit mit den Nanokristallen. Das ergibt ein weißes, fluffiges Pulver. „Damit könnte man zum Beispiel Leichtbauteile herstellen“, sagt Jaekel. Dann zeigt sie getrocknete Filme aus reiner Nanocellulose. Besonders bei kleinen Kristallen sieht der Film ganz klar aus. Im Licht schillert er in allen Regenbogenfarben (Abb. E).
Schließlich führt die Chemikerin ein Stück Altpapier vor, wie es für Lebensmittelverpackungen verwendet wird. Es ist mit den Cellulose-Nanokristallen beschichtet. Seit Wochen steht nun schon eine kleine Ölpfütze darauf, ohne durchzusickern. Das zeigt: Diese biologisch abbaubare Beschichtung könnte Lebensmittel vor Mineralölspuren schützen.
„Holz hat unsere Kultur geprägt“, sagt Svitlana Filonenko. Seit Jahrtausenden ist es Brenn- und Baustoff. Bedrucktes Papier begründete unsere Informationskultur. Im 19. Jahrhundert kam mit Zelluloid der erste Kunststoff auf, und mit ihm der Film als neues Medium. Nun könnte aus Cellulose eine nachhaltige Nanotechnologie entstehen. Das ist das Ziel der Potsdamer Forscherinnen.
Abbildungshinweise:
Titelbild © Adobe Stock, HN; istock / catalby
Abb. A: Nanowelt © R. Wengenmayr; MPG
Abb. B: Cellulose-Baustein © E. Jaekel, MPI für Kolloid- und Grenzflächenforschung / CC BY-NC-ND 4.0
Abb. C: Vom Baum zum Cellulose-Kristall
C1: © R. Wengenmayr / CC BY-NC-SA 4.0
C2: © MPI für Kolloid- und Grenzflächenforschung / CC BY-NC-ND 4.0
Abb. D: Hydrogel © Dr. Nieves Lopez Salas
Abb. E: Schillernde Cellulose-Filme © Dr. Nieves Lopez Salas
Der Text wird unter CC BY-NC-SA 4.0 veröffentlicht.
TECHMAX Ausgabe 28, Winter 2020; Autor: Roland Wengenmayr; Redaktion: Tanja Fendt